« Pensez comme des ingénieurs !« . Voilà une phrase que je répète souvent en stage afin de sensibiliser les apprenants à « comprendre comment ça fonctionne pour savoir comment agir« . Et il est de ces sujets qui méritent cette véritable approche lorsque l’on parle de prise en charge pré-hospitalière, surtout en contexte dégradé, et c’est le cas du choc hémorragique et plus particulièrement de ce que l’on appelle la triade létale.
Comprendre ces mécanismes porte un nom: La physiopathologie.
La physiopathologie est l’étude des mécanismes fonctionnels par lesquels une maladie ou une lésion perturbe l’équilibre normal de l’organisme (homéostasie). Elle établit le lien entre l’étiologie ( les causes et origines de la « maladie ») et ses conséquences observables ( signes clinique).
Cet article est volontairement dense afin de vous offrir une vision approfondie des processus à l’œuvre dans le corps humain lors d’un choc hémorragique : les mécanismes qui se déclenchent, les compensations mises en place, et la raison pour laquelle vous adoptez certains gestes. Notamment, pourquoi il est important de prévenir l’hypothermie dans ce contexte.
Promis, après cette lecture, vous ne verrez plus votre couverture de survie de la même façon !
La Triade létale, qu’est ce que c’est ?
Certains l’appelle également « Triade de la mort« , il s’agit de trois conditions physiopathologiques interconnectées, un cercle vicieux, qui peut conduire au décès du patient si aucunes actions appropriées n’est mises en place dans un certain délai, variable en fonction de l’état initial de la victime. Celles ci sont l’hypothermie, l’acidose métabolique et la coagulopathie. Un bon dessin valant mieux qu’un -trop- long discours, voici un schéma décrivant cette (in)fameuse triade létale:
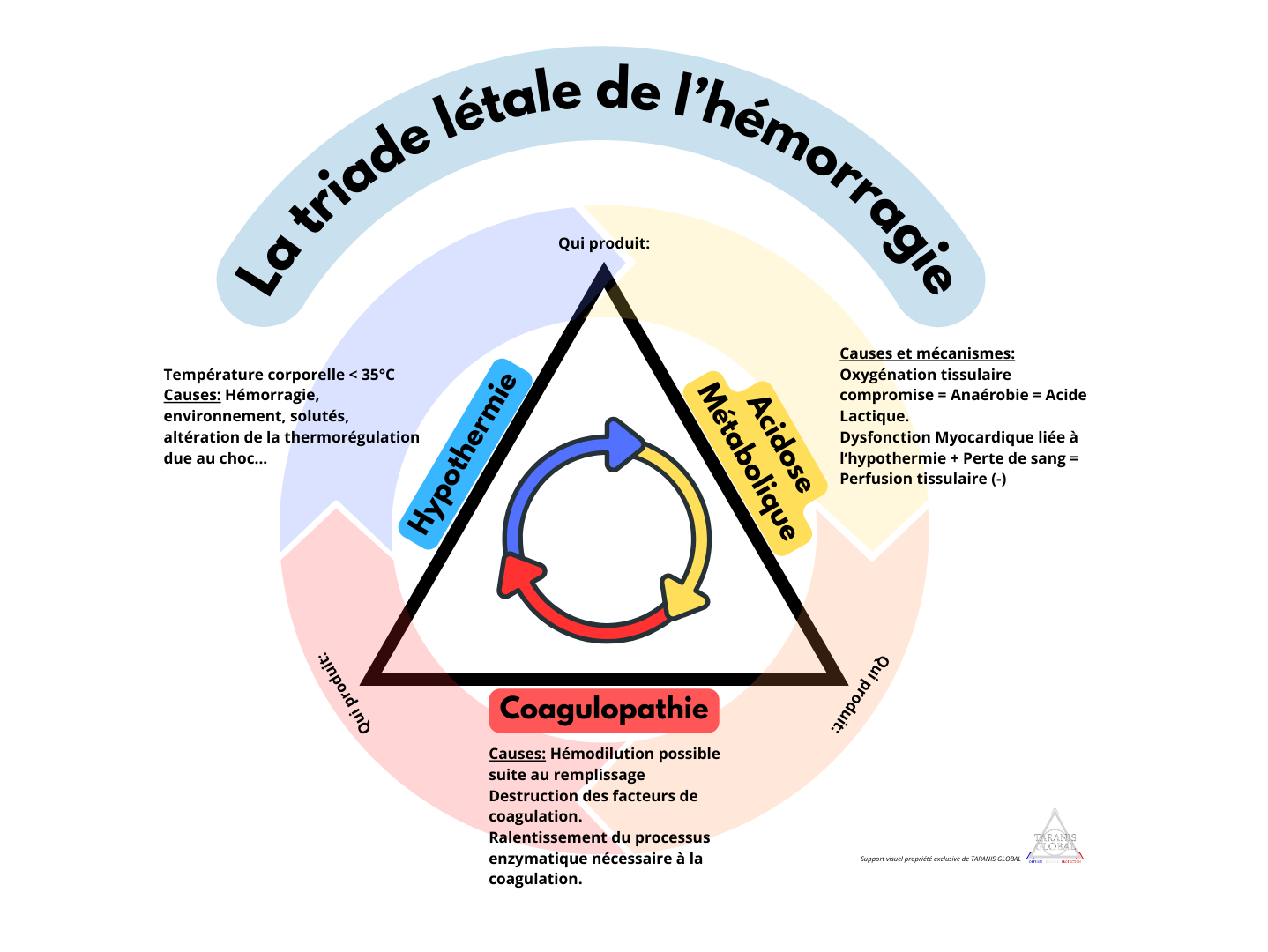
Lorsqu’un patient est victime d’une hémorragie, celui ci commence à perdre de la température corporelle, c’est ici le point d’entrée dans ce cercle vicieux.
Observons d’abord par quels mécanismes physiopathologiques et biochimiques cela se produit. Accrochez-vous, on va rentrer dans le dur !
Physiopathologie de la Perte de Température lors d’un Choc Hémorragique
Perte de Chaleur par Mécanismes Physiques
Une hémorragie entraine une baisse de la température corporelle par plusieurs mécanismes.
Tout d’abord, la diminution du volume sanguin circulant.
- À savoir que le sang est le principal vecteur de chaleur dans l’organisme, une perte de volume sanguin diminue la capacité à distribuer la chaleur aux tissus.
- Une diminution du débit cardiaque réduit la perfusion périphérique, et de ce fait, aggrave la dissipation thermique
Le corps étant une machine formidable, celui ci va mettre en place des mécanismes compensateurs.
- En réponse à l’hypovolémie (baisse du volume sanguin), le système nerveux sympathique déclenche une vasoconstriction pour préserver la perfusion des organes vitaux (cerveau, cœur). (Voir)
- Cette vasoconstriction cutanée et musculaire réduit la production de chaleur en limitant la circulation sanguine aux extrémités. Les mains et les pieds deviennent alors froids, le temps de recoloration cutanée (TRC) commence à augmenter.
En causes externes, nous pourrions ajouter que la victime est exposée à son environnement, et au regard de son état, y est plus exposée (sols froids, vent, humidité…), le sang s’évaporant de la peau de la victime accélère la perte calorique par convection. Lors de la prise en charge, l’administration de solutés froids non réchauffés aggravera encore un peu plus cette chute de température corporelle.
Effets Biochimiques de l’Hémorragie sur la Régulation Thermique
L’hémorragie perturbe les systèmes biochimiques maintenant une température corporelle stable (homéothermie).
Dysfonction du Centre Thermorégulateur
- Le centre hypothalamique, régulateur principal de la température (entre autre), est hypoperfusé en cas de choc.
- Cette hypoperfusion entraîne une altération du signal nerveux maintenant la production de chaleur. Il ne joue plus son rôle de centre régulateur.
Diminution de la Thermogenèse Métabolique
Diminution de la production d’ATP
- Le choc hémorragique entraîne une hypoxie cellulaire (Apport en oxygène insuffisant).
- La production d’ATP (adénosine triphosphate) par phosphorylation oxydative diminue ce qui engendre une baisse du métabolisme basal donc moins de chaleur produite. (source)
Le métabolisme passe alors à un fonctionnement en anaérobie.
- Le manque d’oxygène force les cellules à utiliser la glycolyse anaérobie ( fractionnement des glucides pour produire de l’énergie).
- Ce métabolisme produit moins d’ATP et favorise l’accumulation d’acide lactique
- Une acidose inhibe les enzymes impliquées dans la thermogenèse et le métabolisme mitochondrial.
Altération des hormones thermogéniques
- Le stress physiologique entraîne une libération d’adrénaline et de cortisol, mais la perte sanguine limite leur effet.
- Les hormones thyroïdiennes (T4 convertie en T3), qui régulent, entre autre, la production de chaleur, sont moins actives en raison de la mauvaise perfusion des tissus endocriniens.
Comme vous pouvez le constater, la chute de la température de la victime, considérée comme étant une hypothermie en dessous de 35 °C, ne se limite pas à une sensation de froid et d’inconfort pour le patient. Un ensemble de réactions et de mécanismes en cascade se mettent à l’œuvre, qui vont aggraver son état, et l’attirer inexorablement vers… la mort.
L’acidose métabolique
En conséquence directe de cette perte de chaleur, l’équilibre acido-basique s’en trouve perturbé. L’acidose métabolique correspond à une diminution du pH sanguin (< 7,35) associée à une diminution du bicarbonate plasmatique.
Origine de l’Acidose dans l’Hémorragie
Hypoperfusion et Métabolisme Anaérobie
- La perte de sang réduit la pression artérielle et le débit cardiaque.
- La perfusion des organes diminue : les tissus ne reçoivent plus assez d’oxygène pour fonctionner en aérobie.
- Les cellules passent alors au métabolisme anaérobie, qui produit :
- Acide lactique
- Moins d’ATP, donc inefficacité cellulaire
- Chute du pH intra- et extra-cellulaire
Accumulation de Lactate
- L’acide lactique est normalement métabolisé par le foie (cycle de Cori).
- En cas d’hypoperfusion hépatique, ce recyclage est ralenti, favorisant l’acidose lactique.
- Le lactate plasmatique devient un marqueur de gravité dans le choc hémorragique.
Mécanismes Biochimiques de l’Acidose Métabolique
Réactions clés :
Nous constaterons ici la réaction de glycolyse anaérobie, c’est-à-dire la transformation d’une molécule de glucose en deux molécules d’acide lactique. Pendant cette transformation, des ions H⁺ sont libérés et s’accumulent, ce qui entraîne une diminution du pH sanguin.
C6H12O6 (glucose) → 2 CH3CHOHCOOH (acide lactique)
→ Production d’ions H⁺ → Baisse du pH sanguin
Impact cellulaire :
- Inhibition enzymatique dans les mitochondries (cycle de Krebs, chaîne respiratoire)
- Baisse de la production d’ATP
- Hausse du stress oxydatif
- Hausse de la perméabilité membranaire, ce qui engendre une fuite ionique
- Risque de lyse cellulaire et de défaillance multiviscérale
Vous l’avez compris, cette acidose induite par l’hémorragie en elle même et aggravé par l’hypothermie va engendré un autre phénomène: La coagulopathie.
La coagulopathie
Pour mieux comprendre le principe de coagulopathie, il faut aborder ce que l’on appelle « la cascade de coagulation ».
La Cascade de Coagulation : Un Processus en 3 Phases
Elle repose sur une série d’activation enzymatique qui transforme un saignement en un caillot stable. Elle comprend trois grandes étapes :
Hémostase Primaire (Formation du Clou Plaquettaire)
- Lorsqu’un vaisseau sanguin est lésé, les plaquettes adhèrent à la paroi grâce au facteur de von Willebrand.
- Elles s’activent et s’agrègent pour former un clou plaquettaire temporaire (hémostase primaire).
- Ce clou est fragile et doit être stabilisé par la fibrine, produite lors de l’hémostase secondaire.
Hémostase Secondaire (Cascade de Coagulation)
La cascade de coagulation implique une activation séquentielle de protéines appelées facteurs de coagulation, qui aboutit à la formation de fibrine, stabilisant ainsi le caillot.
Elle suit deux voies principales qui convergent vers une voie commune :
Voie Extrinsèque (Facteur Tissulaire)
- Déclenchée par une lésion externe des vaisseaux.
- Le facteur tissulaire (FT ou Facteur III) libéré par les cellules lésées active le facteur VII, qui active ensuite le facteur X.
- Cette voie est rapide, mais produit peu de thrombine.
Voie Intrinsèque (Contact Sanguin)
- Déclenchée par un dommage interne des vaisseaux sanguins.
- Le facteur XII (Hageman) active une cascade impliquant les facteurs XI, IX et VIII, qui activent ensuite le facteur X.
- Cette voie est plus lente, mais produit beaucoup plus de thrombine.
Voie Commune (Production de Fibrine)
- Le facteur X activé (Xa) transforme la prothrombine (facteur II) en thrombine.
- La thrombine convertit le fibrinogène (facteur I) en fibrine, qui forme un réseau stabilisant le caillot.
- Le facteur XIII consolide les liaisons entre les fibres de fibrine, rendant le caillot plus solide.
Fibrinolyse (Dissolution du Caillot)
Une fois la guérison avancée, le corps doit éliminer le caillot :
- La plasminogène est activée en plasmine, une enzyme qui dégrade la fibrine et dissout le caillot.
- Cela évite l’obstruction prolongée du vaisseau et favorise la cicatrisation.
Une vidéo illustre ce paragraphe plus en détail en suivant ce lien.
La coagulopathie est donc un dysfonctionnement du système hémostatique entraînant une incapacité à former un caillot efficace pour arrêter l’hémorragie.
Physiopathologie : Mécanismes Intriqués
Activation systémique de la coagulation
- Lors d’un traumatisme sévère, les cellules endothéliales sont lésées :
- Libération de facteurs tissulaires (TF)
- Déclenchement de la voie extrinsèque de la coagulation
- Cela provoque une activation massive de la thrombine (FIIa) pour la formation initiale de caillots
- Mais cette activation non contrôlée épuise rapidement :
- Les facteurs de coagulation
- Le fibrinogène
- Les plaquettes
Hyperfibrinolyse
- L’activation de la protéine C (Inhibiteur de la coagulation) par la thrombomoduline endothéliale dégrade :
- Facteurs Va et VIIIa → inhibition de la coagulation
- Hausse des Plasminogène → ↑ plasminogène activator (t-PA) → plasmin → fibrinolyse excessive
- Résultat : Destruction prématurée des caillots
Hypothermie
- Elle ralentit les réactions enzymatiques de la coagulation (en particulier < 34°C)
- Perturbe l’agrégation plaquettaire
- Amplifie les troubles hémostatiques
Acidose
- pH < 7,2 réduit significativement l’activité enzymatique des facteurs de coagulation
- Inhibe la production de thrombine
- Altère l’adhésion et l’activation plaquettaire
Dilution
- L’administration excessive de solutés cristalloïdes ou colloïdes dilue :
- Les facteurs de coagulation
- Le fibrinogène
- Les plaquettes
- Résultat : hémostase inefficace
Consommation et carences
- Les saignements massifs entraine une consommation rapide des facteurs
- Carence en calcium (cofacteur enzymatique) si perfusion avec citrates entrainera une réduction de la coagulation
Pour aller plus loin
Prévenir cette Triade Létale.
Agissant toujours dans le cadre du Damage Control, vous allez « traiter en premier ce qui tue en premier« .
Il est donc prioritaire de stopper l’hémorragie. On ne perd pas de temps en pré-hospitalier, c’est l’hémostase qui sauve le patient, ou du moins, qui augmente grandement ses chances de survie.
Cependant, une fois le « robinet fermé », les conséquences de cette perte de volume sanguin subsistent !
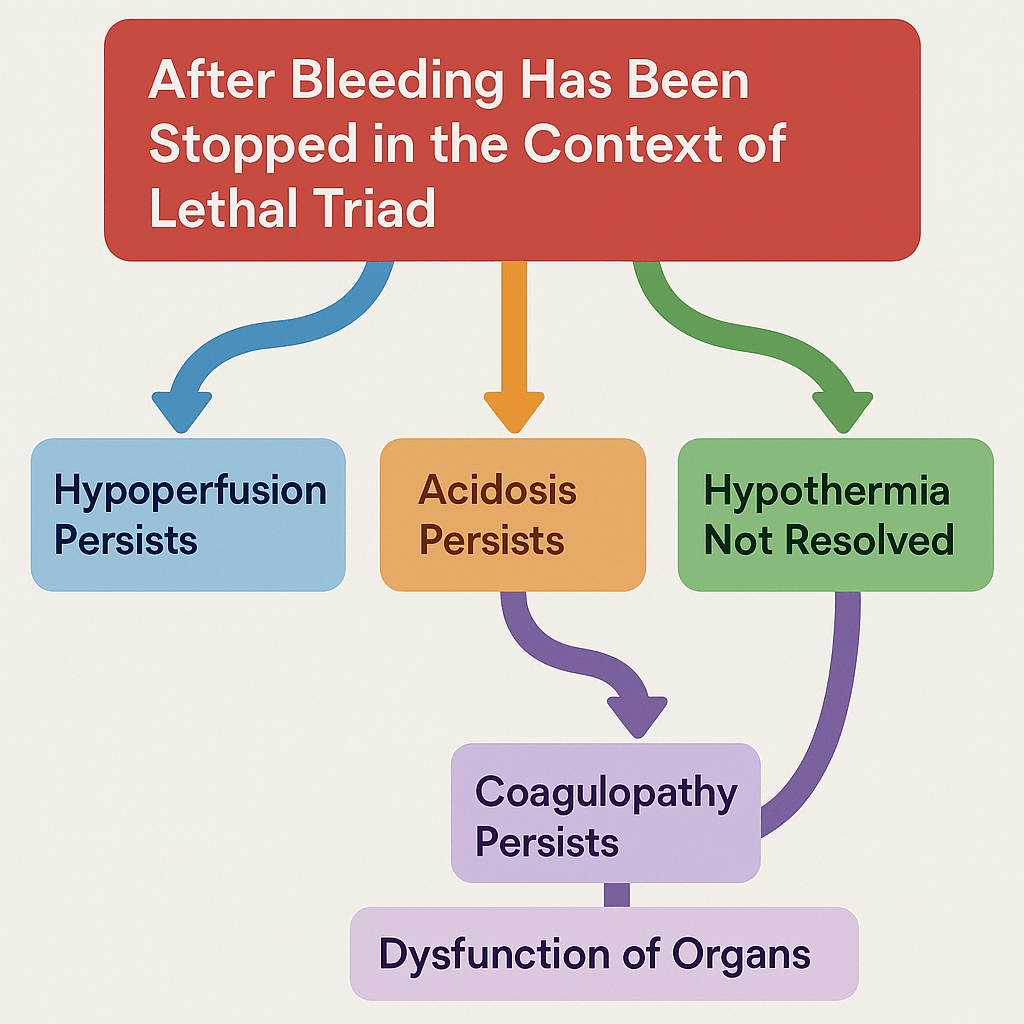
Comme je le disais en début de cet article: « Pensez comme des ingénieurs !« . Maintenant que vous savez comment tout cela fonctionne, voyons comment régler ces problèmes.
En pré-hospitalier
Après avoir stopper le saignement, il va falloir protéger la victime du froid. Pour cela il existe plusieurs solutions, matériels, techniques et astuces que vous allez pouvoir utiliser. Je ferais un focus sur ce point en fin d’article.
Un accès veineux sera simultanément posé (si personnel formé et habilité). En cas d’echec en périphérique (2 fois), un dispositif IO (intra osseux) sera utilisé.
Les différents moyens et objectifs thérapeutiques sont décris dans le tableau ci dessous.
| Phase | Objectifs | Moyens thérapeutiques |
|---|---|---|
| Pré-hospitalier Remote damage control | Stopper le saignement | – Garrot – Compression manuelle – Pansements hémostatiques ± procoagulants – Suture cutanée – Ceinture pelvienne |
| Éviter l’hypothermie | – Protéger du froid et/ou de la pluie – Isoler du sol – Limiter le temps à l’extérieur – Sécher et couvrir – Vecteur de transport chauffé – Solutés chauffés | |
| Accès veineux | – 2 VVP ≥ 18 G- Intraosseux (épaule > tibia) si 2 échecs VVP | |
| Hypotension permissive | – Objectif PAS > 80 mmHg (ou > 100 mmHg si TCG) – Remplissage : 1–1,5 L de cristalloïdes (NaCl 0.9 % ou Ringer Lactate) – Noradrénaline précoce | |
| Antifibrinolyse | – Acide tranexamique < 3 h post-trauma :→ 1 g IV sur 10 min, puis 1 g sur 8 h | |
| Coordination vers plateau technique | – Régulation vers un centre adapté (chirurgie, endovasculaire) | |
| ⚠️ Priorité absolue | « Le geste d’hémostase sauve, pas le remplissage » |
Sur la structure de soins
| Phase | Objectifs | Moyens thérapeutiques |
|---|---|---|
| À l’hôpital Damage control resuscitation | Réanimation et bilan lésionnel | – Suivi hémodynamique et thermique – Réchauffement actif (objectif T° > 34 °C) – Réchauffer les produits transfusés |
| Soutien tensionnel | – Amines (selon objectifs tensionnels) | |
| Transfusion massive | – CGR pour Hb cible 7–9 g/dL – PFC ou plasma lyophilisé (ratio 1:1 avec CGR)- Fibrinogène > 1,5 g/L – Plaquettes > 50 000 (ou > 100 000 si TCG) | |
| Équilibre métabolique | – pH cible > 7,2 – Calcium ionisé > 1 mmol/L : gluconate ou chlorure de calcium | |
| Chirurgie ou radiologie interventionnelle | – Damage control surgery (DCS) – Hémostase chirurgicale rapide – Hémostase endovasculaire (embolisation) |
FOCUS: Gérer l’hypothermie, un geste à la portée de tout secouriste !
Que ce soit dans nos stages ou chez des confrères, j’ai souvent remarqué une chose. Lors des ateliers et exercices pratiques, les apprenants ont souvent tendance à « caser » la gestion de l’hypothermie au second plan. Le geste que l’on réalise « à la fin » de l’action de secours. La cerise sur le gâteau pour montrer « qu’on a tout bien fait ».
Pire encore, parfois cette gestion de la température corporelle est tout simplement occultée ou réduite à la simple pose d’une couverture de « survie » sur la victime.
En effet, même dans le protocole MARCHE, la gestion de l’hypothermie vient après pas mal de choses.
Et pourtant… Les algorithmes et protocoles, indiquent évidemment un ordre de priorité afin d’être en accords avec la philosophie du Damage Control, mais rien n’empêche de faire les choses simultanément !
Voir même de les anticiper !
Maintenant que vous connaissez de manière approfondie ce mécanisme de triade létale, vous avez clairement compris la nécessité absolue d’éviter que la victime se refroidisse. Cela doit devenir automatique: « Je coupe le robinet, je regarde que l’air passe dans les tuyaux, et pendant que je prépare le reste, je fais en sorte que la victime se réchauffe ou à minima, qu’elle ne se refroidisse pas plus.«
Comment lutter contre l’hypothermie ?
Les moyens improvisés:
Isoler du sol : c’est la priorité. Le sol aspire la chaleur corporelle par conduction. Un corps en contact direct avec le sol perd deux fois plus de chaleur que par l’air (convection).
Utilisez une veste, un sac, une chemise, un carton, un tapis de voiture, tout ce qui crée une couche isolante.
Limiter l’exposition à l’air : le vent et les mouvements d’air accélèrent les pertes thermiques. Protégez au maximum la victime avec ce que vous avez sous la main.
Sécher et déshabiller en cas d’humidité : si la victime est mouillée, les pertes de chaleur sont massives et très rapides. Il est préférable de retirer les vêtements mouillés et de sécher la peau, avant de la couvrir à nouveau.
Position allongée, au chaud : si la victime est consciente, mobilisable, et sans suspicion de traumatisme rachidien ou crânien, déplacez-la dans un endroit abrité (hall d’immeuble, pièce chauffée, etc..). Allongez-la, car cela limite la demande cardiaque et prévient les malaises liés à la perfusion défaillante des organes.
Utiliser les ressources du groupe : chaque personne autour de vous a potentiellement une veste, un vêtement, ou une ressource thermique à prêter !
La couverture de survie:
Les couvertures de survie sont des incontournables des kit de premiers secours. La plus connue d’entre elles est certainement la couverture en alu, doré et argenté, que l’on voit partout. Cependant, son efficacité, et la technique de pose enseignée depuis de nombreuses années sont largement remises en question de nos jours. J’ai d’ailleurs écrit un article à ce sujet ici.
À savoir que toutes les couvertures de survie ne se valent pas ! Il existe aujourd’hui des couvertures chauffantes très performante et qui ne prennent que peu de place. C’est le cas par exemple du HPMK-I de North American Rescue. Vous trouverez un descriptif de ce produit ici.

Les chaufferettes
Un indispensable à avoir selon moi dans son sac, les chaufferettes permettrons d’aider à maintenir la température corporelle de la victime à un niveau acceptable, permettra d’aider à réchauffer vos solutés, mais également vous protègera de l’hypothermie en auto sauvetage !
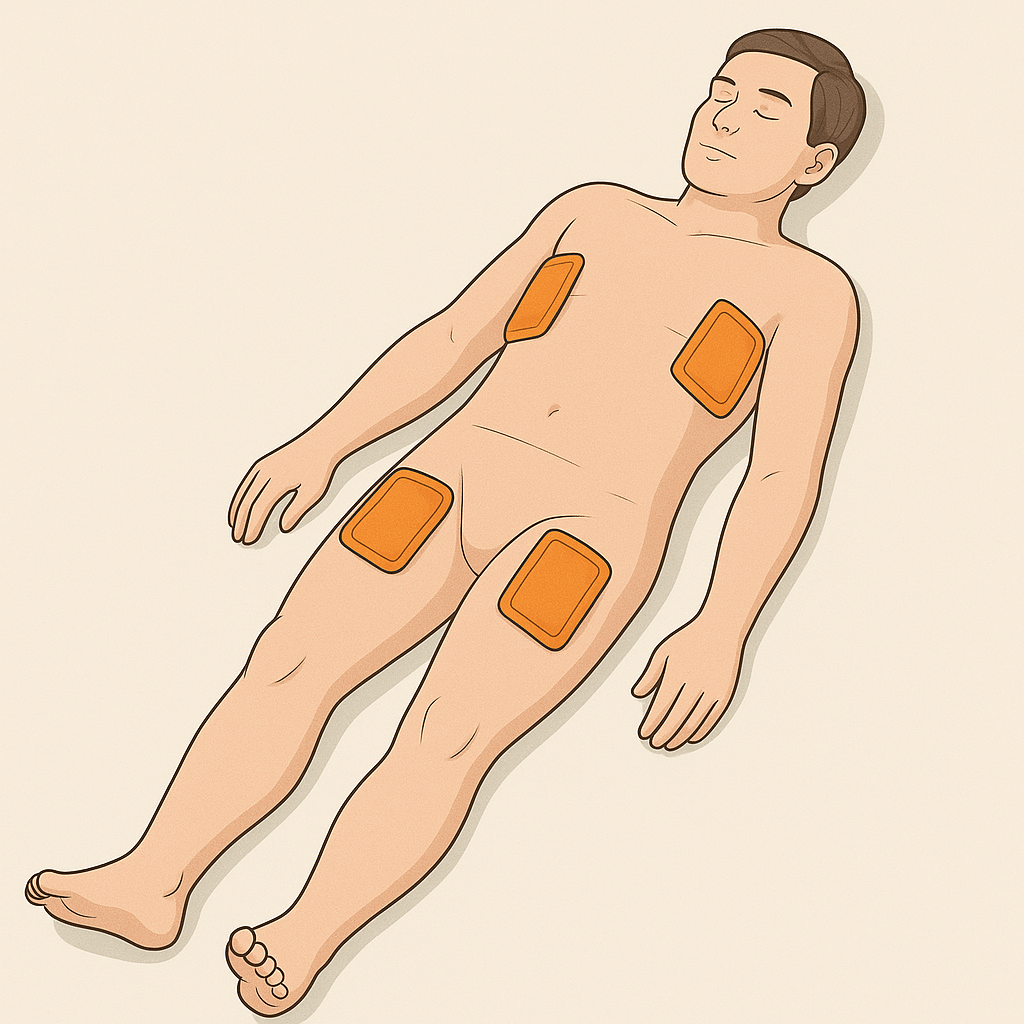
L’idée est de les placer aux plis de l’aine et des aisselles, au contact de l’artère fémorale et humérale.
Pour réchauffer les fluides, placez votre poche en « sandwich » entre deux chaufferettes, maintenus par du sparadrap.
Références et remerciements:
Je remercie grandement le Docteur THELLIER Dimitri, pour son aide concernant la cascade de coagulation ainsi que pour les ressources médicale transmises, qui m’ont grandement aidées à la rédaction de cet article. Dr THELLIER est également consultant et formateur, pour en savoir plus voici le lien de son site internet DTMEDS.
[1] Levrat A, Defournel C, Savary D, David JS. Anomalies de la coagulation et traumatisme grave. Urgences 2010;54:619-37.
[2] Cosgriff N, Moore EE, Sauaia A, et al. Predicting life-threatening coagulopathy in the massevely transfused trauma patient: hypothermia and acidoses revisited. J Trauma 1997;42(5):857-62.
[3] Evans JA, van Wessem KJP, McDougall D, et al. Epidemiology of traumatic deaths: comprehensive population-based assessment. World J Surg 2010;34(1):158-63.
[4] Fröhlich M, Mutschler M, Caspers M, et al. Trauma-induced coagulopathy upon emergency room arrival: still a significant problem despite increased awareness and management? Eur J Trauma Emerg Surg 2019;45(1):115-24.
[5] Meng ZH, Wolberg AS, Monroe DM 3rd, Hoffman M. The effect of temperature and pH on the activity of factor VIIa: implications for the efficacy of high-dose factor VIIa in hypothermic and acidotic patients. J Trauma 2003;55(5):886-91.
[6] Ferrara A, MacArthur JD, Wright HK, et al. Hypothermia and acidosis worsen coagulopathy in the patient requiring massive transfusion. Am J Surg 1990;160(5):515-8.
[7] Pottecher J, Lefort H, Adam P, et al. Guidelines for the acute care of severe limb trauma patients. Anaesth Crit Care Pain Med 2021. À paraître.
[8] Garrigue-Huet D, Ausset S, Bliem C, et al. Indications de transfusion de plasmas lyophilisés (Plyo) chez un patient en choc hémorragique ou à risque de transfusion massive en milieu civil (adulte, enfant et nouveauné). Société française d’anesthésie et de réanimation. 2020. https://sfar.org/download/indications-detransfusion-de-plasmas-lyophilises-plyo-chez-un-patient-en-choc-hemorragique-ou-a-risque-de-transfusionmassive-en-milieu-civil-adulte-enfant-et-nouveau-ne/?wpdmdl=30312&refresh=60b3b651930081622390353.
[9] Malgras B, Prunet B, Lesaffre X, et al. Damage control: concept and implementation. J Visc Surg 2017;154 Suppl 1:S19-29.
[10] Julien C, Chauvin A, Didelot N, et al. Pansements hémostatiques procoagulants et hémorragies. Rev Infirm 2021;70(273):23-6.

